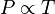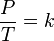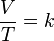from : wikipedia indonesia
Gerak Brown adalah gerakan terus menerus suatu partikel zat cair atau zat gas. Artinya partikel partikel ini tidak pernah dalam keadaan stasioner atau sepenuhnya diam. Pertama kali dibuktikan dan dicetuskan oleh Robert Brown seorang ahli botani skotlandia pada tahun 1827. Prinzipnya mudah sekali, Brown mengamati partikel di bawah mikroskop dan dia mengamati pergerakan terus menerus dari partikel-partikel kecil tersebut, yang mana geraknya makin cepat bila temperaturnya makin tinggi. Gerak ini dapat diamati pada zat cair kolloid atau gas. Di dalam suatu ruang pergerakan partikel gas tersebut (analogie terhadap zat cair juga) tidak teratur dan bergerak bebas, dengan kata lain partikel gas itu bergerak dengan kecepatan yang berbeda-beda. Bila partikel gas tersebut menabrak partikel gas lain atau tembok dinding ruang, maka kecepatan serta arah vektornya pun ikut berubah. Penyebaran kecepatannya dapat dirumuskan dengan penyebaran kecepatan Maxwell atau dengan kata lain Penyebaran kecepatan Maxwell memberikan gambaran tentang kecepatan partikel bergerak tergantung dari temperatur ruang(lingkungan) tersebut.
Kecepatan rata-rata pergerakan molekul di udara adalah 500m/s atau 1800 km/h. Kecepatan ini melebihi kecepatan gelombang bunyi yang besarnya 330 m/s. Energi dari partikel gas ideal juga tergantung dari suhu udara. Teori gas kinetik memberikan hubungan proporsional antara energi rata2 kinetik dengan temperatur gas.
Diperoleh dari "http://id.wikipedia.org/wiki/Gerak_Brown"
Hukum gas ideal
Ditulis oleh Yoshito Takeuchi pada 11-08-2008
from : http://www.chem-is-try.org/
Gas merupakan satu dari tiga wujud zat dan walaupun wujud ini merupakan bagian tak terpisahkan dari studi kimia, bab ini terutama hanya akan membahasa hubungan antara volume, temperatur dan tekanan baik dalam gas ideal maupun dalam gas nyata, dan teori kinetik molekular gas, dan tidak secara langsung kimia. Bahasan utamanya terutama tentang perubahan fisika, dan reaksi kimianya tidak didisuksikan. Namun, sifat fisik gas bergantung pada struktur molekul gasnya dan sifat kimia gas juga bergantung pada strukturnya. Perilaku gas yang ada sebagai molekul tunggal adalah contoh yang baik kebergantungan sifat makroskopik pada struktur mikroskopik.
Sifat gas
Sifat-sifat gas dapat dirangkumkan sebagai berikut.
Gas bersifat transparan.
Gas terdistribusi merata dalam ruang apapun bentuk ruangnya.
Gas dalam ruang akan memberikan tekanan ke dinding.
Volume sejumlah gas sama dengan volume wadahnya. Bila gas tidak diwadahi, volume gas akan menjadi tak hingga besarnya, dan tekanannya akan menjadi tak hingga kecilnya.
Gas berdifusi ke segala arah tidak peduli ada atau tidak tekanan luar.
Bila dua atau lebih gas bercampur, gas-gas itu akan terdistribusi merata.
Gas dapat ditekan dengan tekanan luar. Bila tekanan luar dikurangi, gas akan mengembang.
Bila dipanaskan gas akan mengembang, bila didinginkan akan mengkerut.
Dari berbagai sifat di atas, yang paling penting adalah tekanan gas. Misalkan suatu cairan memenuhi wadah. Bila cairan didinginkan dan volumenya berkurang, cairan itu tidak akan memenuhi wadah lagi. Namun, gas selalu akan memenuhi ruang tidak peduli berapapun suhunya. Yang akan berubah adalah tekanannya.
Alat yang digunakan untuk mengukur tekanan gas adalah manometer. Prototipe alat pengukur tekanan atmosfer, barometer, diciptakan oleh Torricelli.
Tekanan didefinisikan gaya per satuan luas, jadi tekanan = gaya/luas.
Dalam SI, satuan gaya adalah Newton (N), satuan luas m2, dan satuan tekanan adalah Pascal (Pa). 1 atm kira-kira sama dengan tekanan 1013 hPa.
1 atm = 1,01325 x 105 Pa = 1013,25 hPa
Namun, dalam satuan non-SI unit, Torr, kira-kira 1/760 dari 1 atm, sering digunakan untuk mengukur perubahan tekanan dalam reaksi kimia.
Volume dan tekanan
Fakta bahwa volume gas berubah bila tekanannya berubah telah diamati sejak abad 17 oleh Torricelli dan filsuf /saintis Perancis Blase Pascal (1623-1662). Boyle mengamati bahwa dengan mengenakan tekanan dengan sejumlah volume tertentu merkuri, volume gas, yang terjebak dalam tabung delas yang tertutup di salah satu ujungnya, akan berkurang. Dalam percobaan ini, volume gas diukur pada tekanan lebih besar dari 1 atm.
Boyle membuat pompa vakum menggunakan teknik tercangih yang ada waktu itu, dan ia mengamati bahwa gas pada tekanan di bawah 1 atm akan mengembang. Setelah ia melakukan banyak percobaan, Boyle mengusulkan persamaan (6.1) untuk menggambarkan hubungan antara volume V dan tekanan P gas. Hubungan ini disebut dengan hukum Boyle.
PV = k (suatu tetapan) (6.1)
Penampilan grafis dari percobaan Boyle dapat dilakukan dengan dua cara. Bila P diplot sebagai ordinat dan V sebagai absis, didapatkan hiperbola (Gambar 6.1(a)). Kedua bila V diplot terhadap 1/P, akan didapatkan garis lurus (Gambar 6.1(b)).
(a) Plot hasil percobaan; tekanan vs. volume(b) Plot hasil percobaan; volume vs 1/tekanan. Catat bahwa kemiringan k tetap.
Volume dan temperatur
Setelah lebih dari satu abad penemuan Boyle ilmuwan mulai tertarik pada hubungan antara volume dan temperatur gas. Mungkin karena balon termal menjadi topik pembicaraan di kotakota waktu itu. Kimiawan Perancis Jacques Alexandre César Charles (1746-1823), seorang navigator balon yang terkenal pada waktu itu, mengenali bahwa, pada tekanan tetap, volume gas akan meningkat bila temperaturnya dinaikkan. Hubungan ini disebut dengan hukum Charles, walaupun datanya sebenarnya tidak kuantitatif. Gay-Lussac lah yang kemudian memplotkan volume gas terhadap temperatur dan mendapatkan garis lurus (Gambar 6.2). Karena alasan ini hukum Charles sering dinamakan hukum Gay-Lussac. Baik hukum Charles dan hukum Gay-Lussac kira-kira diikuti oleh semua gas selama tidak terjadi pengembunan.
Pembahasan menarik dapat dilakukan dengan hukum Charles. Dengan mengekstrapolasikan plot volume gas terhadap temperatur, volumes menjadi nol pada temperatur tertentu. Menarik bahwa temperatur saat volumenya menjadi nol sekiatar -273°C (nilai tepatnya adalah -273.2 °C) untuk semua gas. Ini mengindikasikan bahwa pada tekanan tetap, dua garis lurus yang didapatkan dari pengeplotan volume V1 dan V2 dua gas 1 dan 2 terhadap temperatur akan berpotongan di V = 0.
Fisikawan Inggris Lord Kelvin (William Thomson (1824-1907)) megusulkan pada temperatur ini temperatur molekul gas menjadi setara dengan molekul tanpa gerakan dan dengan demikian volumenya menjadi dapat diabaikan dibandingkan dengan volumenya pada temperatur kamar, dan ia mengusulkan skala temperatur baru, skala temperatur Kelvin, yang didefinisikan dengan persamaan berikut.
273,2 + °C = K (6.2)
Kini temperatur Kelvin K disebut dengan temperatur absolut, dan 0 K disebut dengan titik nol absolut. Dengan menggunakan skala temperatur absolut, hukum Charles dapat diungkapkan dengan persamaan sederhana
V = bT (K) (6.3)
dengan b adalah konstanta yang tidak bergantung jenis gas.
Menurut Kelvin, temperatur adalah ukuran gerakan molekular. Dari sudut pandang ini, nol absolut khususnya menarik karena pada temperatur ini, gerakan molekular gas akan berhenti. Nol absolut tidak pernah dicapai dengan percobaan. Temperatur terendah yang pernah dicapai adalah sekitar 0,000001 K.
Avogadro menyatakan bahwa gas-gas bervolume sama, pada temperatur dan tekanan yang sama, akan mengandung jumlah molekul yang sama (hukum Avogadro; Bab 1.2(b)). Hal ini sama dengan menyatakan bahwa volume real gas apapun sangat kecil dibandingkan dengan volume yang ditempatinya. Bila anggapan ini benar, volume gas sebanding dengan jumlah molekul gas dalam ruang tersebut. Jadi, massa relatif, yakni massa molekul atau massa atom gas, dengan mudah didapat.
Persamaan gas ideal
Esensi ketiga hukum gas di atas dirangkumkan di bawah ini. Menurut tiga hukum ini, hubungan antara temperatur T, tekanan P dan volume V sejumlah n mol gas dengan terlihat.
Tiga hukum Gas
Hukum Boyle: V = a/P (pada T, n tetap) Hukum Charles: V = b.T (pada P, n tetap) Hukum Avogadro: V = c.n (pada T, P tetap)
Jadi, V sebanding dengan T dan n, dan berbanding terbalik pada P. Hubungan ini dapat digabungkan menjadi satu persamaan:
V = RTn/P (6.4)
atau
PV = nRT (6.5)
R adalah tetapan baru. Persamaan di atas disebut dengan persamaan keadaan gas ideal atau lebih sederhana persamaan gas ideal.
Nilai R bila n = 1 disebut dengan konstanta gas, yang merupakan satu dari konstanta fundamental fisika. Nilai R beragam bergantung pada satuan yang digunakan. Dalam sistem metrik, R = 8,2056 x10–2 dm3 atm mol-1 K-1. Kini, nilai R = 8,3145 J mol-1 K-1 lebih sering digunakan.
Latihan 6.1 Persamaan gas ideal
Sampel metana bermassa 0,06 g memiliki volume 950 cm3 pada temperatur 25°C. Tentukan tekanan gas dalam Pa atau atm).
Jawab: Karena massa molekul CH4 adalah 16,04, jumlah zat n diberikan sebagai n = 0,60 g/16,04 g mol-1 = 3,74 x 10-2 mol. Maka, P = nRT/V = (3,74 x10-2 mol)(8,314 J mol-1 K-1) (298 K)/ 950 x 10-6 m3)= 9,75 x 104 J m-3 = 9,75 x 104 N m-2= 9,75 x 104 Pa = 0,962 atm
Dengan bantuan tetapan gas, massa molekul relatif gas dapat dengan mudah ditentukan bila massa w, volume V dan tekanan P diketahui nilainya. Bila massa molar gas adalah M (g mol-1), akan diperoleh persamaan (6.6) karena n = w/M.
PV = wRT/M (6.6)
maka
M = wRT/PV (6.7)
Latihan 6.2 Massa molekular gas
Massa wadah tertutup dengan volume 0,500 dm3 adalah 38,7340 g, dan massanya meningkat menjadi 39,3135 g setelah wadah diisi dengan udara pada temperatur 24 °C dan tekanan 1 atm. Dengan menganggap gas ideal (berlaku persamaan (6.5)), hitung "seolah" massa molekul udara.
Jawab: 28,2. Karena ini sangat mudah detail penyelesaiannya tidak diberikan. Anda dapat mendapatkan nilai yang sama dari komposisi udara (kira-kira N2:O2 = 4:1).
Hukum tekanan parsial
Dalam banyak kasus Anda tidak akan berhadapan dengan gas murni tetapi dengan campuran gas yang mengandung dua atau lebih gas. Dalton tertarik dengan masalah kelembaban dan dengan demikian tertarik pada udara basah, yakni campuran udara dengan uap air. Ia menurunkan hubungan berikut dengan menganggap masing-masing gas dalam campuran berperilaku independen satu sama lain.
Anggap satu campuran dua jenis gas A (nA mol) dan B (nB mol) memiliki volume V pada temperatur T. Persamaan berikut dapat diberikan untuk masing-masing gas.
pA = nART/V (6.8)
pB = nBRT/V (6.9)
pA dan pB disebut dengan tekanan parsial gas A dan gas B. Tekanan parsial adalah tekanan yang akan diberikan oleh gas tertentu dalam campuran seandainya gas tersebut sepenuhnya mengisi wadah.
Dalton meyatakan hukum tekanan parsial yang menyatakan tekanan total P gas sama dengan jumlah tekanan parsial kedua gas. Jadi,
P = pA + pB = (nA + nB)RT/V (6.10)
Hukum ini mengindikasikan bahwa dalam campuran gas masing-masing komponen memberikan tekanan yang independen satu sama lain. Walaupun ada beberapa gas dalam wadah yang sama, tekanan yang diberikan masing-masing tidak dipengaruhi oleh kehadiran gas lain.
Bila fraksi molar gas A, xA, dalam campuran xA = nA/(nA + nB), maka pA dapat juga dinyatakan dengan xA.
pA = [nA/(nA + nB)]P (6.11)
Dengan kata lain, tekanan parsial setiap komponen gas adalah hasil kali fraksi mol, xA, dan tekanan total P.
Tekanan uap jenuh (atau dengan singkat disebut tekanan jenuh) air disefinisikan sebagai tekanan parsial maksimum yang dapat diberikan oleh uap air pada temperatur tertentu dalam campuran air dan uap air. Bila terdapat lebih banyak uap air, semua air tidak dapat bertahan di uap dan sebagian akan mengembun.
Latihan 6.3 Hukum tekanan parsial
Sebuah wadah bervolume 3,0 dm3 mengandung karbon dioksida CO2 pada tekanan 200 kPa, dansatu lagi wadah bervolume 1,0 dm3 mengandung N2 pada tekanan 300 kPa. Bila kedua gas dipindahkan ke wadah 1,5 dm3. Hitung tekanan total campuran gas. Temperatur dipertahankan tetap selama percobaan.
Jawab: Tekanan parsial CO2 akan menjadi 400 kPa karena volume wadah baru 1/2 volume wadah sementara tekanan N2 adalah 300 x (2/3) = 200 kPa karena volumenya kini hanya 2/3 volume awalnya. Maka tekanan totalnya 400 + 200 = 600 kPa.